Всеволод Елагин. Графика и проза на сайте
Всеволод Елагин. Графика и проза на сайте P.S. Смеющая заметить женщина, любите книжки читать? Так книжки же, как и художественные фильмы, творческие люди пишут. Чем острее написали, тем больше продажи книг, гонорар жирнее. А правда или нет, не важно!
Матвиенко пообещала, что «закручивания гаек» и возвращения тоталитаризма не будет
Да ты чё! А мужики-то не знают...
В Ледовой Академии «Высота» впервые в истории Озёрска прошел праздник фигурного катания «Тодес» на «Высоте»
Матвиенко пообещала, что «закручивания гаек» и возвращения тоталитаризма не будет
Матвиенко пообещала, что «закручивания гаек» и возвращения тоталитаризма не будет
12 килограмм крышек собрал филиал РИР в Озёрске в рамках проекта #КрышкиДобра
В Госдуме предложили запретить продажу алкоголя в майские праздники
Возврата к тем временам нет и не будет.
P.S. И смею заметить, что я - женщина, поэтому несколько приструните в себе свой лагерный жаргон. Матвиенко пообещала, что «закручивания гаек» и возвращения тоталитаризма не будет

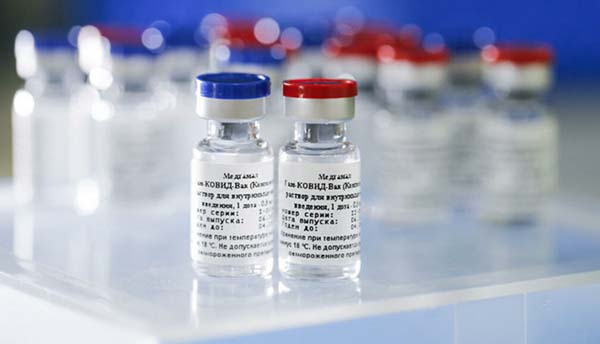
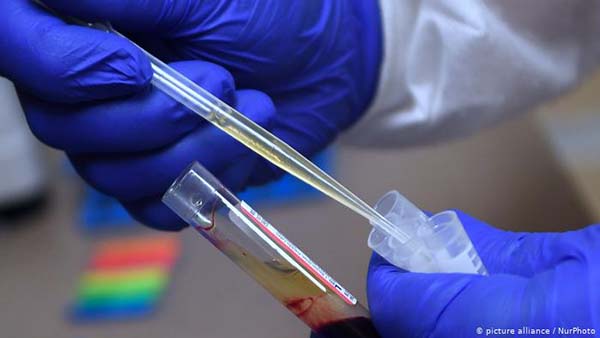
Вакцина «Спутник V»: разработчики не подтвердили соответствие нормам ЕС, сообщает Reuters
Масла в огонь вокруг споров по поводу ковидной вакцины «Спутник V», разработанной в России, подлила публикация Reuters. Источники агентства рассказали, с чем связана задержка одобрения вакцины в Европе.
Европейское агентство лекарственных средств (EMA) не может оценить вакцину «Спутник V» из-за того, что разработчики неоднократно не предоставляли данные, необходимые европейскому регулятору для утверждения препарата. Об этом говорят источники агентства.
Ранее Reuters сообщало, что одобрение вакцины «Спутник V» может быть отложено до осени или даже до конца года. Причина - к началу июня регулятор все еще не получил производственных данных по вакцине, а те клинические сведения, что были предоставлены, оказались неполными. В частности, ЕМА не получило формы отчетов о побочных эффектах, которые наблюдались у участников испытаний вакцины. Еще регулятору неясно, как отслеживались результаты участников испытаний, получавших плацебо.
Исследование «Спутника V», которое проводилось во Франции, вызвало новый вопрос. Разработчики вакцины «Спутник V» не подтвердили, оказывается, документально, что основной банк клеток — исходный строительный блок вакцины — соответствует нормам ЕС по предотвращению заражения болезнями.
По данным источников международного агентства, европейский регулятор оценивает нарушения в отношении российской вакцины по шкале от «незначительные» до «критические».
В то же время один из собеседников Reuters уточнил: в Европе нет оснований сомневаться, что «Спутник V» — безопасная и эффективная вакцина. Исследование, опубликованное в журнале Lancet в феврале, показало, что эффективность российской вакцины превышает 90%.
В Российском фонде прямых инвестиций (РФПИ), который продвигает вакцину «Спутник V», агентству Reuters сообщили, что инспекторы EMA уже посетили производственные объекты, где выпускается вакцина. По результатам проверок не предъявлено серьезных претензий.
Печать 28.04, 10:12
Вербное воскресенье отмечают православные христиане 28 апреля
28.04, 10:12
Вербное воскресенье отмечают православные христиане 28 апреля
 27.04, 12:16
В Челябинской области отменены первомайские шествия и праздничные салюты
27.04, 12:16
В Челябинской области отменены первомайские шествия и праздничные салюты
 27.04, 10:15
Кремль отказался обсуждать особняк замминистра обороны
27.04, 10:15
Кремль отказался обсуждать особняк замминистра обороны
 27.04, 09:43
Лазареву субботу отмечают православные христиане 27 апреля
27.04, 09:43
Лазареву субботу отмечают православные христиане 27 апреля
 27.04, 06:59
Гороскоп на 27 апреля 2024 года
27.04, 06:59
Гороскоп на 27 апреля 2024 года
 26.04, 13:39
Аркаим приглашает южноуральцев на открытие туристического сезона
26.04, 13:39
Аркаим приглашает южноуральцев на открытие туристического сезона
 26.04, 10:58
Вместо молока — денежная компенсация. Сколько можно получить на вредных производствах?
26.04, 10:58
Вместо молока — денежная компенсация. Сколько можно получить на вредных производствах?
 26.04, 10:17
Сумма взятки в деле замминистра обороны Иванова - 1 млрд. рублей
26.04, 10:17
Сумма взятки в деле замминистра обороны Иванова - 1 млрд. рублей
 26.04, 10:00
Патрушев увидел в нелегальной миграции риск распада страны
26.04, 10:00
Патрушев увидел в нелегальной миграции риск распада страны
 26.04, 08:43
В России хотят запретить массовые обзвоны
26.04, 08:43
В России хотят запретить массовые обзвоны
 26.04, 08:38
Какая погода ожидает южноуральцев в выходные?
26.04, 08:38
Какая погода ожидает южноуральцев в выходные?
 26.04, 07:03
Гороскоп на 26 апреля 2024 года
26.04, 07:03
Гороскоп на 26 апреля 2024 года
 25.04, 12:23
В Челябинской области выпал снег
25.04, 12:23
В Челябинской области выпал снег
 25.04, 10:33
Патриарх Кирилл запретил в служении священника, который отпевал Навального*
25.04, 10:33
Патриарх Кирилл запретил в служении священника, который отпевал Навального*
 25.04, 09:58
Взятки заместителю Шойгу оценили в миллиард рублей
25.04, 09:58
Взятки заместителю Шойгу оценили в миллиард рублей
 25.04, 06:58
Гороскоп на 25 апреля 2024 года
25.04, 06:58
Гороскоп на 25 апреля 2024 года
 24.04, 12:46
На Южном Урале появится особая экономическая зона
24.04, 12:46
На Южном Урале появится особая экономическая зона
 24.04, 10:39
В Москве задержали заместителя Шойгу
24.04, 10:39
В Москве задержали заместителя Шойгу
 24.04, 08:52
В России создали центр для изъятия книг из продажи
24.04, 08:52
В России создали центр для изъятия книг из продажи
 24.04, 08:22
Экс-владельцы ЧЭМК и «Арианта» не смогли снять арест со своего имущества
24.04, 08:22
Экс-владельцы ЧЭМК и «Арианта» не смогли снять арест со своего имущества